★千葉中央駅校開校!Instagramはじめました★
フォローお願いします👇
https://www.instagram.com/premium_chibachuou
大学受験のあれこれを投稿していきます☆
=======================
こんにちは。
八千代緑が丘校の轟です。
生徒から化学についての融点についての質問から
始まったこのシリーズですが今日は第4話。
昨日は共有結合について書きましたが
今日は金属結合に書きます。
第1話
http://www.jasmec.co.jp/cgi-bin/diaryopen/diaryopen02/diary.cgi?no=2937
第2話
http://www.jasmec.co.jp/cgi-bin/diaryopen/diaryopen02/diary.cgi?no=2939
第3話
http://www.jasmec.co.jp/cgi-bin/diaryopen/diaryopen02/diary.cgi?no=2940
金属元素であるナトリウムNaを例に考えてみます。
Na原子の最外殻は以図の電子配置をしています。
(つまり、3s軌道に電子が1つ入っており、
3つの3p軌道が空の状態。)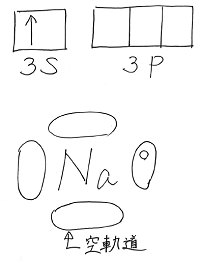
その電子配置の状態を上図にように表すとします
さて、この原子同士を結合すると、何が起こるでしょうか?
「それは金属結合でしょ~」と即答せずに、
第3話の共有結合の話を基に考えてみて下さい。
NaはHと同じように最大殻に電子を1個だけ持つんですよ。
H同士はどのように結合しましたっけ?
お互いの1s軌道を連結させて分子軌道を作ったんでしたよね?
ということは、同じく最大殻に電子を1個だけ持つNa同士だって
お互いの3s軌道同士を連結させて分子軌道を作り、
Na-Naという共有結合を作って分子となると考えるのが
自然ではないでしょうか?
つまり下図のように状態1⇒状態2になります。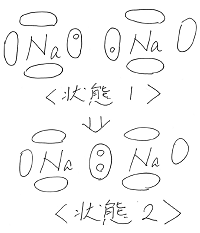
(:が2つの電子を表し、〇は軌道を表しています。
2つの軌道が合わさって〇の中に:がある状態。
他の中が空の〇は空軌道となっている3p軌道を
表しています。)
ここで皆さんの声が聞こえてきそうです。
「そんなわけないっしょ!?
だって教科書に金属結合するって書いてあるじゃん!!」
まぁまぁその気持ちを抑えて…。
最終的にはそうなるんですけど、
今回皆さんに知って頂きたいのは
「どのようなプロセスで金属結合に至るのか。
どのようなプロセスで共有電子対になりそうな
電子が自由電子になるのか」
という点なんです。
===========================
<八千代緑が丘 校舎紹介ページ>
http://www.jasmec.co.jp/koushaguide/pym.htm
八千代緑が丘校ではいつでも無料で個別学習相談
を行っています。
勉強で困っていることのある方はいつでもおっしゃって下さい。
個別学習相談のお申込みはこちらから👇
https://www.jasmec.co.jp/toshin/reserve/premium_reserve.htm
===========================
上の図ではNa原子を2つだけ描いたのですが、Na-Naでつながって
一旦分子になったとすると、これらの分子は分子間力
(分子間力については最終回で説明予定)
で互いに集まり、状態3をつくるようになります。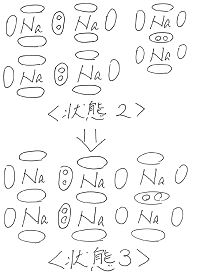
この状態3で注目すべきことは、空の軌道の重なりが
実に多いということです。
勿論、この空の軌道の中には電子がないため、
合体した空軌道をはさむNa原子の間に結合は生じません。
しかし、もしこの中に電子が入ってくれば、
この間に結合が生じることになります。
ところで、Naは第1イオン化エネルギーが相対的に小さいため、
最外殻電子が原子核から離れることはそれほど困難ではありません。
そこで、電子は一旦満席になった軌道から、
空軌道に移動することが可能となります。
その結果、一度状態3ができると、
電子は次々と別の空軌道の中を移動し
状態3 ⇔ 状態4 ⇔ 状態5
のような結合状態に至ります。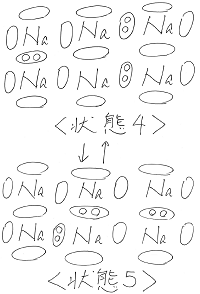
このとき、Naの集団は、全体がつながた状態になります。
もはや、この中にはNa-Naの分子は存在しません。
このような状態は、陽イオンの集合を、自由に動き回る電子(自由電子)
がつなぎとめていると捉えることができます。
この結合を金属結合と呼びます。
このようなストーリーを経て、H-Hとは異なり、
電子が自由に動き回ることができ、それによって
電気的な力でマイナスの電気を持つ電子がプラスの電気を持つ原子核
をつないでいるわけです。
ですから、金属結合となる原子の特徴は
空軌道を多く持ち、またイオン化エネルギーがあまり大きくない
ことが挙げられます。
今回で、少し金属結合の見方が変わったのではないでしょうか。
瞬間で捉えると、自由電子同士が共有電子対を作って
結合しているわけです。
そして次々と共有電子対を作るペアが変わるので、
長い目で見ると、電子が動き、その動く電子が
原子同士をつなぎとめているように見えているわけなんです。
では、次回の第5話で「1族元素(アルカリ金属)の単体の融点は
原子番号が大きくなるに従って低くなる」ことの理由について、
そして第6回(これが最終話)で「17族元素(ハロゲン)、18族元素(希ガス)
の単体の融点は原子番号が大きくなるに従って高くなる」
ことの理由について書きたいと思います。
また次回も読んで頂ければ幸いです。
(八千代緑が丘校 轟)
=======================
★一日体験・個別説明会受付中!★
お問い合わせ・お申込みはこちらから👇
https://www.jasmec.co.jp/toshin/reserve/premium_reserve.htm